Соматомедин-С (Инсулиноподобный фактор роста I)
Гормональный посредник действия соматотропного гормона.
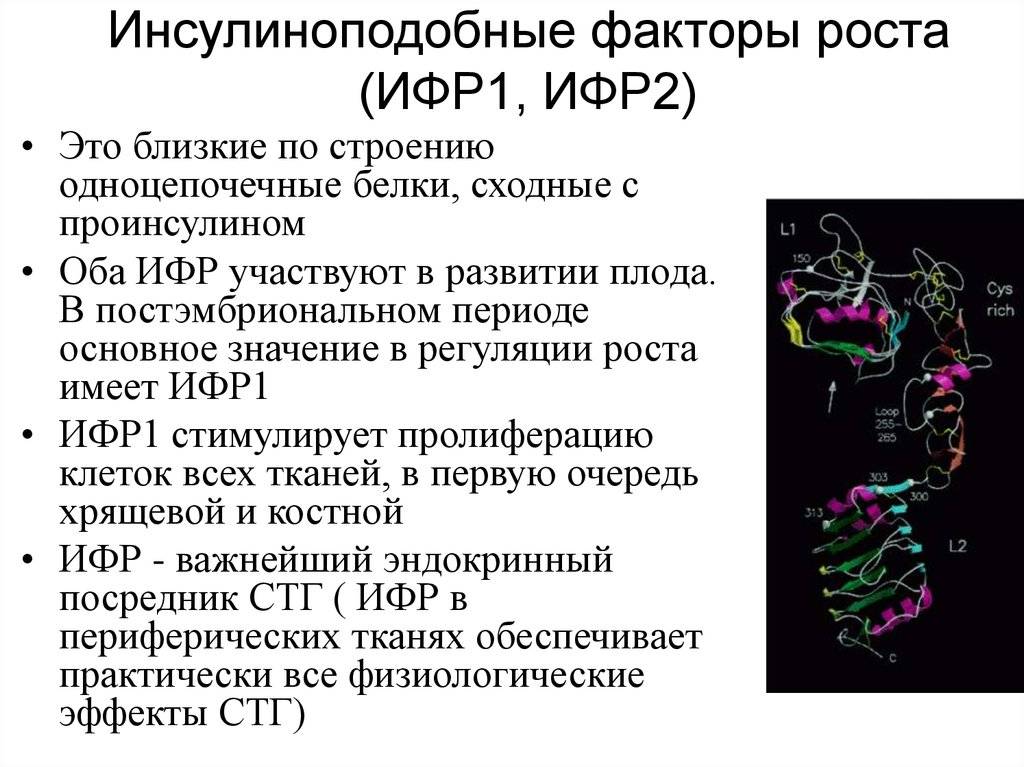
Соматомедин С (инсулиноподобный фактор роста 1 или IGF-1) – одноцепочечный полипептид с молекулярной массой 7 649 Да. Инсулиноподобными эти факторы названы в связи с их способностью стимулировать поглощение глюкозы мышечной и жировой тканью аналогично инсулину. Известен также инсулиноподобный фактор 2 (IGF-2). По структуре IGF-1 гомологичен инсулину и инсулиноподобному фактору роста 2, синтез его идёт преимущественно (но не только) в печени, стимулируется соматотропным гормоном и приёмом пищи. IGF-1 является гормональным посредником действия на ткани соматотропного гормона (см. тест № 99 – соматотропный гормон). Система инсулиноподобных факторов роста, их связывающих белков и рецепторов участвует в процессах, связанных с ростом и развитием организма, поддержанием нормального функционирования многих клеток организма, обладает выраженным антиапоптотическим эффектом. Это одна из наиболее сложных эндокринных систем организма.
Выделено 6 высокоафинных IGF-связывающих белков, активность которых также подвержена регуляции. В крови IGF-1 циркулирует в связанном с белками виде. Время его нахождения в крови больше, чем соматотропного гормона. Одним из важных эффектов IGF-1 является стимуляция роста костей в длину. Циркулирующий IGF-1 повышает чувствительность к инсулину. Сниженный уровень IGF-1 ассоциирован с резистентностью к инсулину (риском развития нарушений углеводного обмена и диабета типа 2). Поскольку IGF-1 играет существенную роль в контроле клеточного цикла и апоптоза (процессах, тесно связанных с механизмами опухолевого роста), в настоящее время интенсивно исследуется его роль в канцерогенезе. При рождении человека IGF-1 в плазме едва определяется, в период детства его уровень градуально растёт, достигая максимума в возрасте от пубертатного периода приблизительно до 40 лет, после чего плавно снижается.
Во время беременности уровень IGF-1 в материнской крови увеличивается.
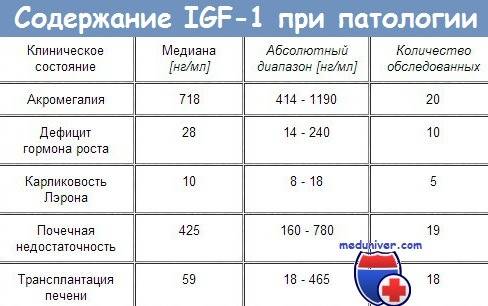
Тестирование IGF-1 применяют при диагностике нарушений роста. Во многих случаях уровень IGF-1 является лучшим маркёром для оценки продукции гормона роста. Нормальный уровень соматомедина С в плазме является строгим свидетельством против дефицита соматотропного гормона. Низкий уровень соматомедина С подразумевает дефицит гормона роста и требует дополнительного тестирования уровня соматотропного гормона для выявления его возможного субнормального уровня. При акромегалии уровень IGF-1 может служить индикатором выраженности заболевания, серийные исследования используют в мониторинге лечения. При карликовости IGF-1 может использоваться для контроля лечения гормоном роста. Измерение IGF-1 полезно также при оценке изменений обменного статуса.
Пределы определения: 3 нг/мл-1500 нг/мл
Взятие крови предпочтительно проводить утром натощак, после 8-14 часов ночного периода голодания (воду пить можно), допустимо днем через 4 часа после легкого приема пищи. Накануне исследования необходимо исключить повышенные психоэмоциональные и физические нагрузки (спортивные тренировки), приём алкоголя, за час до исследования – курение
Важно! Не следует проводить исследование в период острых заболеваний. С общими рекомендациями для подготовки к исследованиям можно ознакомиться
- Диагностика нарушений роста.
- Мониторинг лечения акромегалии и карликовости.
- Оценка изменений обменного статуса.
Интерпретация результатов исследования содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения в медицинском центре СТУДИЯ ДОКТОР и коэффициенты пересчёта: нг/мл.
Референсные значения (нг/мл):
| Возраст | Границы |
до 3 лет | 28 – 131 |
от 3 до 6 лет | 56 – 204 |
от 6 до 10 лет | 85 – 315 |
10 – 13 лет | 95 – 473 |
13 – 16 лет | 213 – 654 |
16 – 18 лет | 195 – 511 |
от 18 до 22 лет | 146 – 472 |
от 22 до 25 лет | 129 – 388 |
от 25 до 30 лет | 121 – 336 |
30 – 35 лет | 125 – 311 |
35 – 40 лет | 111 – 284 |
40 – 50 лет | 94 – 269 |
50 – 60 лет | 89 – 255 |
более 60 лет | 93 – 224 |
Повышение значений:
- акромегалия;
- синдром Кушинга;
- почечная недостаточность;
- применение лекарственных препаратов (андрогены, клонидин, дексаметазон).
Понижение значений:
- карликовость;
- гипопитуитаризм;
- гипотиреоидизм;
- голодание;
- анорексия;
- синдром эмоциональной депривации;
- карликовость Ларона (в присутствии повышенного уровня гормона роста);
- цирроз печени и другие гепатоцеллюлярные заболевания;
- острые заболевания;
- введение эстрогенов (высокие дозы), тамоксифен.
Инсулиноподобный фактор роста-1
ИФР-1:
- полипептидный гормон, содержащий 70 аминокислот,
- обладает эндокринным, паракринным и аутокринным влиянием,
- является структурным гомологом ИФР-2 и инсулина более чем на 60%,
- около 70% ИФР-1 продуцируется в печени,
- обеспечивает ингибирующий сигнал обратной связи на секрецию ГР в гипоталамусе, стимулируя продукцию соматостатина,
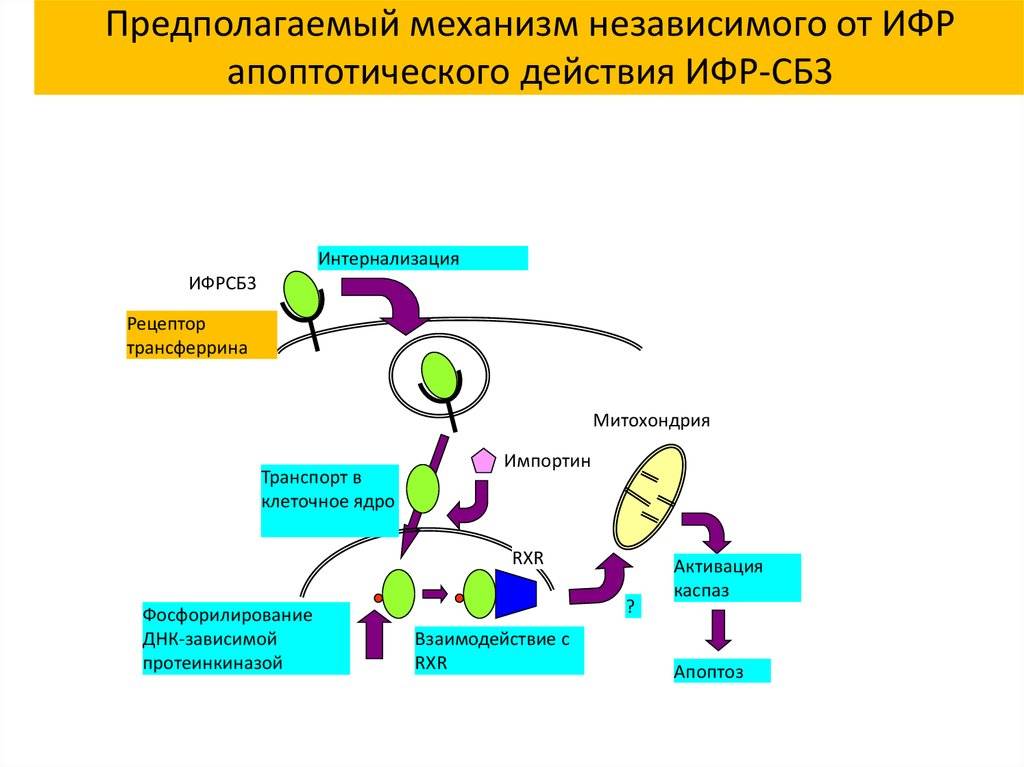
- концентрация ИФР-1 жестко регулируется так называемыми белками, связывающими инсулиноподобный фактор роста (ИФРСБ), регулируя период полураспада этого гормона.
- ИФРСБ могут регулировать активность ИФР-1 как независимый субстрат для рецептора к ИФР-1, так и к другим рецепторам клеток.
- Интересно, что аффинитет ИФРСБ к рецептору выше почти в 6 раз по сравнению с ИФР-1.
- ИФРСБ обладают метаболическими эффектами.
- ИФР-1 может связываться как со своим специфическим рецептором, так и с рецептором к инсулину, но с меньшим аффинитетом.
- Все эти рецепторы обладают тирозин-киназной активностью, то есть являются естественными активаторами Akt.
- Роль ИФР-2 полностью неизвестна, однако точно определено его влияние при развитии плода и протекции головного мозга.
- ИФР-2 может действовать через свой специфический рецептор.
- Обладает также меньшим сродством к рецептору к ИФР-1, инсулину и гибридным рецепторам.
- Рецептор ИФР-2 считается акцептором для секвестрации ИФР-1 и ИФР-2 из внеклеточной среды
- Считается, что ИФР-2 активирует Gaq-белки в кардиомиоцитах.
- В последние десятилетия исследовалась роль и участие ИФР-1 в:
- росте и развитии тканей,
- пролиферации,
- метаболизме жиров,
- противосовпалительной активности,
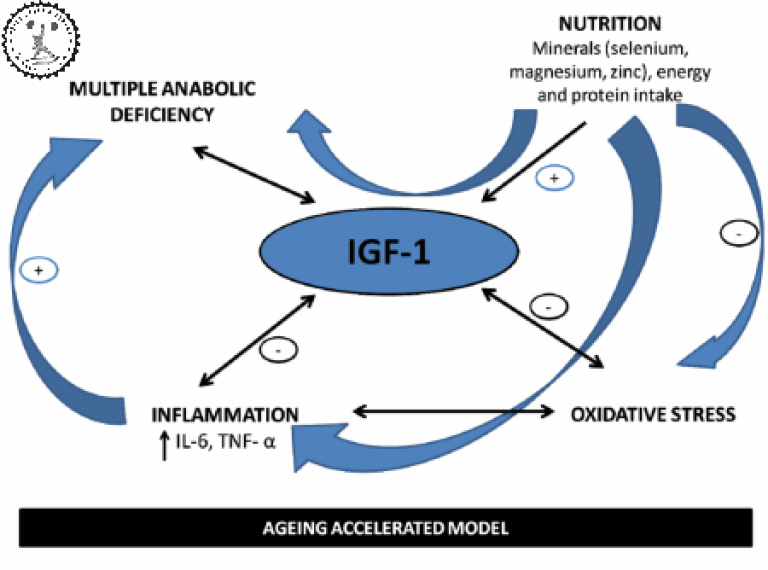
- антиэйджинге,
- анаболической активности,
- анти-оксидантных активности,
- нейро- и гепато-протекции.
- ИФР-1 оказывает защитный эффект для митохондрий, препятствуя их оксидативному поражению.
Инсулиноподобный фактор роста-1 и метаболизм углеводов
- ИФР-1 повышает захват глюкозы в периферических тканях.
- Экзогенный ИФР-1 снижает уровень глюкозы в плазме крови и у здоровых людей, и у пациентов с СД 1 и 2 типа, а также в общем у людей, резистентных к инсулину
- В исследованиях показано, что при резистентности к инулину повышается количество гибридных рецепторов к инсулину/ИФР-1 в мышечной и жировой тканях
- Высокие дозы ИФР-1 обычно приводят к гипогликемии,
- Несмотря на снижение концентрации циркулирующего в крови инсулина.
- В группе мышей с инактивированными генами рецептора инсулина было показано снижение глюкозы в крови при помощи ИФР-1.
- Что свидетельствует о том, что ИФР-1 действует не только через гибридные рецепторы инсулина на метаболизм углеводов, но и через свои специфические рецепторы.
- Позже было пересмотрено действие ИФР-1 на мышцы и установлено прямое влияние на поглощение глюкозы.
- У мышей с инактивированными генами ИФР-1 в печени развивалась резистентность к инсулину.
- В этих условиях происходило повышение концентрации глюкозы и существенное снижение инсулин-индуцированного аутофосфорилирования рецептора к инсулину и ИРС в скелетных мышцах
- После экзогенного введения ИФР-1 всё восстановилось.
- Можно сделать вывод, что печёночная экспрессия ИФР-1 играет ключевую роль в сигнальном каскаде инсулина в скелетных мышцах и поглощении ими глюкозы
- У мышей с инактивированными генами ИФР-1 в печени развивалась резистентность к инсулину.
- При отсутствии гибридных рецепторов и инактивации рецепторов к ИФР-1 в мышцах возникала резистентность к инсулину и СД 2 типа в раннем возрасте.
- Также, вероятно ИФР-1 влияет на глюконеогенез в почках.
- Кроме того, экспрессия рецепторов ИФР-1 была обнаружена и в печени,
- ИФР-1 снижает уровень гормона роста в плазме крови благодаря отрицательной обратной связи.
- Это ведёт к снижению влияния гормона роста на функции печени, в том числе улучшая чувствительность к инсулину.
- Как и в жировой ткани, так и в печени гормон роста инициирует синтез субъединицыPI3K -p85,
- что ведёт к суппрессии активности p110
- Таким образом, ИФР-1 может косвенно влиять на метаболизм углеводов через
- снижение концентрации гормона роста в плазме крови,
- повышение активности инсулина.
- В постпрандиальный период уровень ИФР-1 в крови увеличивается.
- Свободный ИФР-1 способствует:
- окислению жирный кислот в мышцах,
- подавлению гормона роста,
- стимуляции транспорта глюкозы в мышечную ткань,
- подавлению глюконеогенеза в почках.
- ИФР-1-связывающие белки также играю роль в метаболизме углеводов с помощью влияния на ИФР-1.
- ИФР-1-связывающие белки взаимодействуют с ядерным рецептором RXR-α.
- Тот, в свою очередь, реагирует с PPAR-γ,
- ИФР-1-связывающие белки взаимодействуют с ядерным рецептором RXR-α.
- Повышенная экспрессия ИФР-1-связывающих белков ассоциирована с резистентностью к инсулину.
- В исследовании на мышах с неполной секрецией ИФР-1 было показано снижение экспрессии генов, участвующих в метаболизме глюкозы:
- фосфоенолпируваткарбоксилазы-1,
- глюкозо-6-фосфатазы,
- пируватдегидрогеназыкиназы изофермента-4,
- АТФ-цитратлиазы.
- Что приводило к гипергликемии.
- Эти изменения были купированы заместительной терапией низкими дозами ИФР-1 в течении 10 дней.
- Известно, что инсулин повышает экспрессию данных генов.
- Результаты исследования показывают противоположные инсулину эффекты дефицита ИФР-1.
- Свойства ИФР-1 в данном случае не “инсулиноподобны”, а антагонистичны.
- Кроме того, пируватдегидрогеназыкиназы изофермент-4 кодирует пируватдегидрогеназныйкомплекс (ПДК).
- ПДК является новой мишенью при лечении метаболического синдрома с помощью поддержания стабильного содержания АТФ в клетке.
- Это происходит благодаря эффективному использования свободных жирных кислот и глюкозы с помощью ПДК.
- В исследовании на мышах с неполной секрецией ИФР-1 было показано снижение экспрессии генов, участвующих в метаболизме глюкозы:
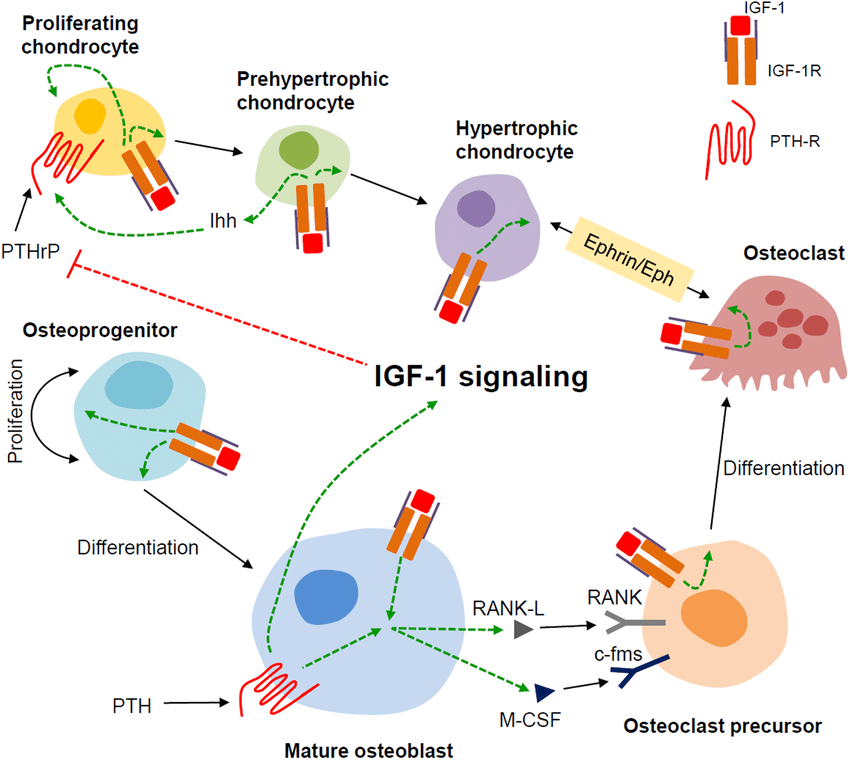
Органы и ткани, пораженные IGF-1
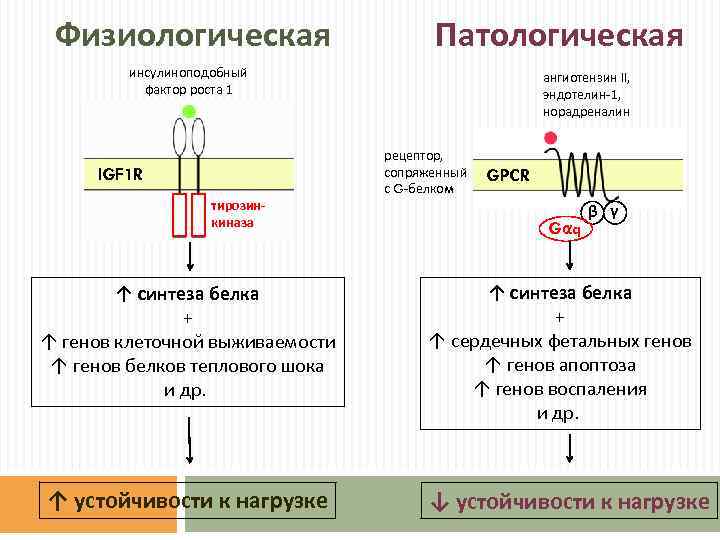
Поскольку многие различные типы тканей экспрессируют рецептор IGF-1, эффекты IGF-1 разнообразны. Он действует как нейротрофический фактор, индуцирующий выживание нейронов. Это может катализировать скелетные мышцы гипертрофия, побуждая синтез белка, и блокируя мышечная атрофия. Он защищает хрящ клеток, и связано с активацией остеоциты, и, таким образом, может быть анаболическим фактором для кость. Поскольку при высоких концентрациях он способен активировать рецептор инсулина, он также может дополнять эффекты инсулин.[нужна цитата] Рецепторы IGF-1 находятся в гладких мышцах сосудов, тогда как типичные рецепторы инсулина не обнаруживаются в гладких мышцах сосудов.
Механизм действия
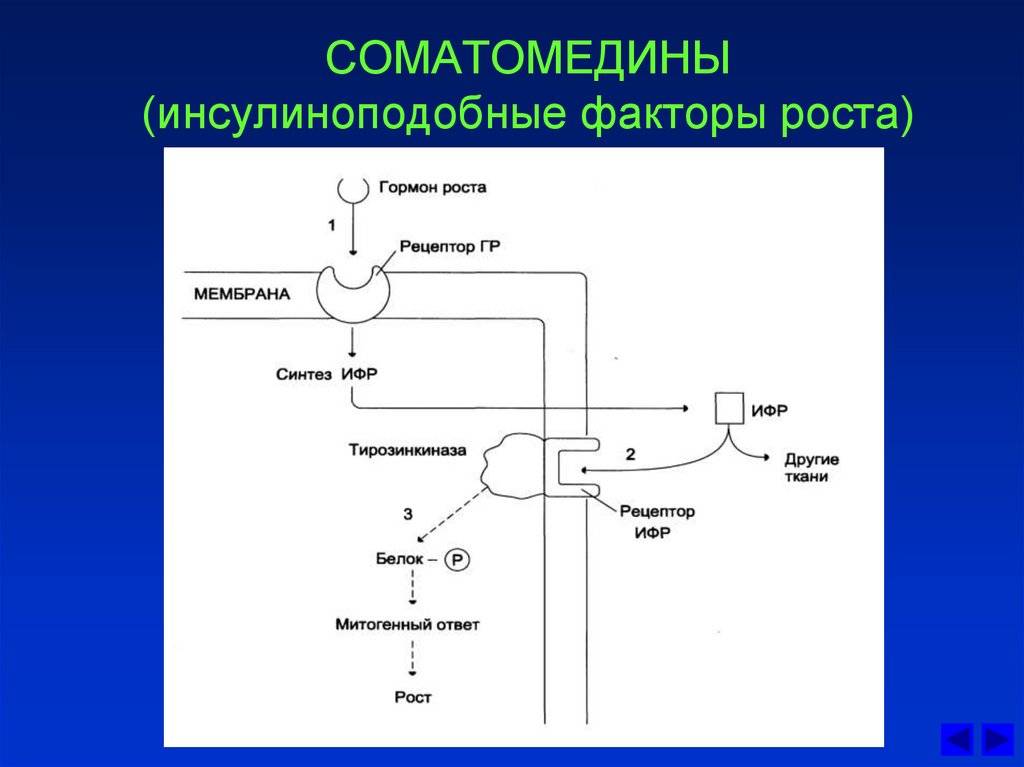
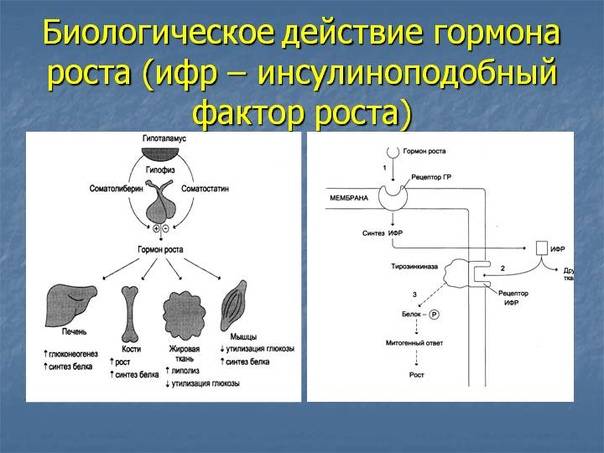
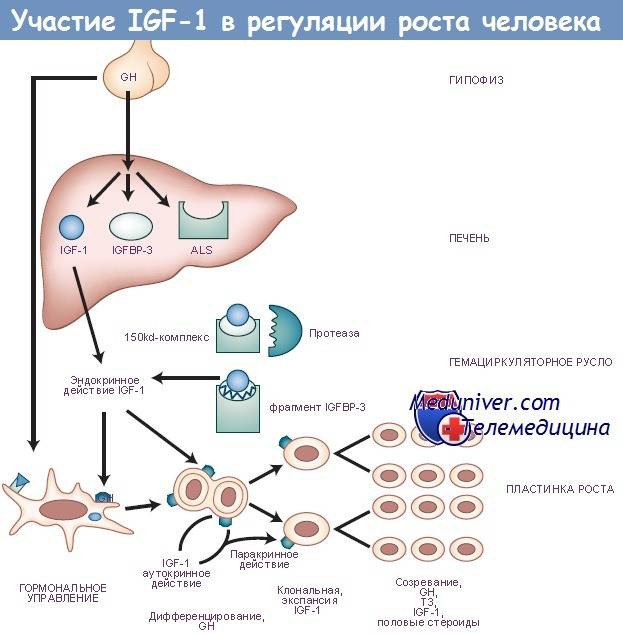
IGF-1 является первичным медиатором действия гормона роста (GH). Гормон роста вырабатывается передней долей гипофиза , попадает в кровоток и затем стимулирует печень к выработке IGF-1. Затем IGF-1 стимулирует системный рост организма и оказывает стимулирующее воздействие на почти все клетки тела, особенно на скелетные мышцы , хрящи , кости , печень , почки , нервы , кожу , кроветворные и легочные клетки. Помимо инсулиноподобных эффектов, IGF-1 также может регулировать синтез клеточной ДНК .
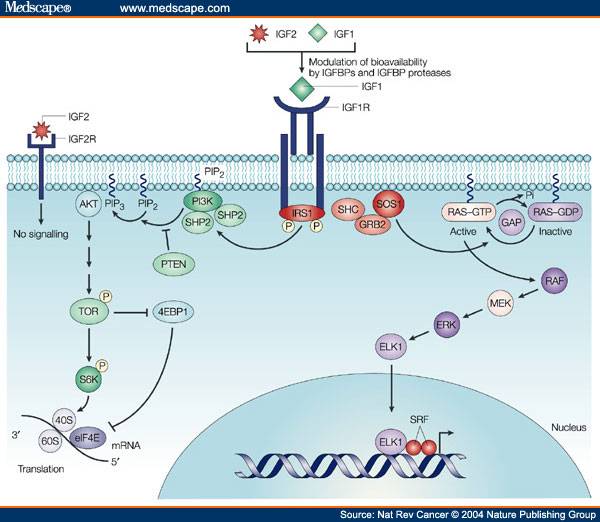
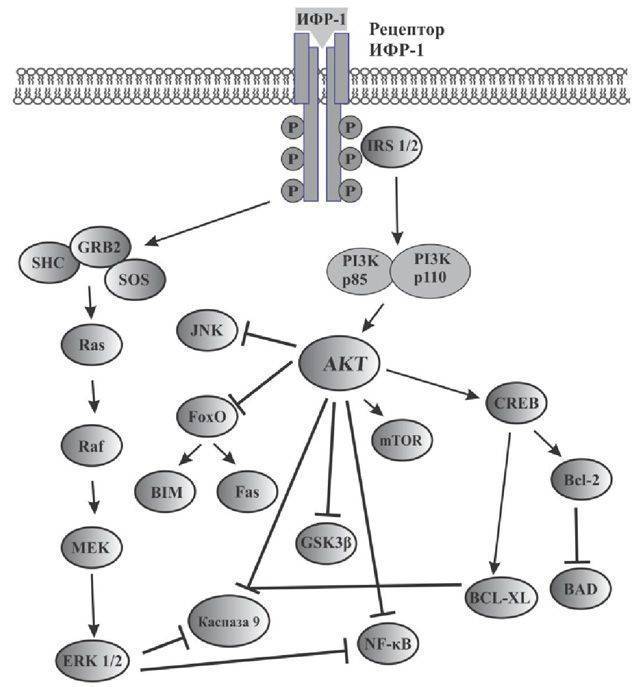
IGF-1 связывается с по меньшей мере , две поверхности клеток рецепторных тирозинкиназ : The ИФР-1 – рецептора (IGF1R) и рецептора инсулина . Его основное действие опосредовано связыванием со специфическим рецептором IGF1R, который присутствует на поверхности многих типов клеток во многих тканях. Связывание с IGF1R инициирует внутриклеточную передачу сигналов. IGF-1 является одним из наиболее мощных природных активаторов сигнального пути AKT , стимулятором роста и пролиферации клеток и мощным ингибитором запрограммированной гибели клеток . Рецептор IGF-1, по-видимому, является «физиологическим» рецептором, потому что он связывает IGF-1 со значительно более высоким сродством, чем рецептор инсулина. IGF-1 активирует рецептор инсулина примерно в 0,1 раза сильнее, чем инсулин. Часть этой передачи сигналов может происходить через гетеродимеры IGF1R / рецептора инсулина (причина путаницы в том, что исследования связывания показывают, что IGF1 связывает рецептор инсулина в 100 раз хуже, чем инсулин, но это не коррелирует с фактической эффективностью IGF1 in vivo. при индуцировании фосфорилирования рецептора инсулина и гипогликемии).
IGF-1 связывает и активирует свой собственный рецептор IGF-1R посредством экспрессии на клеточной поверхности рецепторных тирозинкиназ (RTK) и дальнейшего сигнала через многочисленные каскады внутриклеточной трансдукции. IGF-1R является важнейшим ролевым индуктором в модуляции метаболических эффектов IGF-1 на клеточное старение и выживаемость. В локализованной клетке-мишени IGF-1R опосредует паракринную активность. После его активации происходит инициация внутриклеточной передачи сигналов, вызывая множество сигнальных путей. Важный механистический путь, участвующий в посредничестве каскада, влияет на ключевой путь, регулируемый фосфатидилинозитол-3 киназой ( PI3K ) и ее нижележащим партнером, mTOR (мишень рапамицина млекопитающих). Рапамицин связывается с ферментом FKBPP12, подавляя комплекс mTORC1. mTORC2 остается незатронутым и реагирует повышающим регулированием AKT, управляя сигналами через ингибированный mTORC1. Фосфорилирование эукариотического фактора инициации трансляции 4E ( EIF4E ) с помощью mTOR подавляет способность эукариотического фактора инициации трансляции 4E-связывающего белка 1 ( EIF4EBP1 ) ингибировать EIF4E и замедлять метаболизм. Мутация сигнального пути PI3K-AKT-mTOR является важным фактором образования опухолей, обнаруживаемых преимущественно на коже, внутренних органах и вторичных лимфатических узлах (саркома Капоши). IGF-1R позволяет активировать эти сигнальные пути и впоследствии регулирует клеточное долголетие и метаболический повторный захват биогенных веществ. Терапевтический подход, направленный на уменьшение таких скоплений опухолей, может быть вызван ганитумабом. Ганитумаб представляет собой моноклональное антитело (mAb), антагонистически направленное против IGF-1R. Ганитумаб связывается с IGF-1R, предотвращая связывание IGF-1 и последующий запуск сигнального пути PI3K-mTOR; ингибирование этого пути выживания может привести к подавлению роста опухолевых клеток и индукции апоптоза опухолевых клеток.
Инсулиноподобный фактор роста 1 , как было показано , связываются и взаимодействуют со всеми семь IGF-1 связывающих белков (БСИФР): IGFBP1 , IGFBP2 , IGFBP3 , IGFBP4 , IGFBP5 , IGFBP6 и IGFBP7 . Некоторые IGFBP ингибируют. Например, и IGFBP-2, и IGFBP-5 связывают IGF-1 с более высоким сродством, чем он связывает свой рецептор. Следовательно, повышение уровней этих двух IGFBP в сыворотке приводит к снижению активности IGF-1.
Ось IGF1 / GH
«Ось» IGF также обычно называется осью гормона роста / IGF-1. Инсулиноподобный фактор роста 1 (IGF-1, или иногда с Римская цифра как IGF-I) в основном секретируется печенью в результате стимуляции гормон роста (GH). IGF-1 важен как для регуляции нормальной физиологии, так и для ряда патологических состояний, включая рак. Было показано, что ось IGF играет роль в продвижении распространение клеток и подавление смерть клетки (апоптоз). Инсулиноподобный фактор роста 2 (IGF-2, или иногда как IGF-II) считается основным фактор роста требуется для ранней разработки, пока IGF-1 экспрессия необходима для достижения максимального роста. Джин нокаут исследования на мышах подтвердили это, хотя другие животные, вероятно, регулируют экспрессию этих генов различными способами. Хотя IGF-2 может быть в первую очередь плод в действии он также важен для развития и функционирования таких органов, как мозг, печень, и почка.[нужна цитата]
Факторы, которые, как считается, вызывают колебания уровней GH и IGF-1 в кровообращении, включают генетический состав человека, время дня, возраст, пол, физический статус, уровень стресса, уровень питания и т. Д. индекс массы тела (ИМТ), состояние болезни, раса, эстрогеновый статус и ксенобиотик потребление.
IGF-1 участвует в регулировании нейронное развитие включая нейрогенез, миелинизация, синаптогенез, и дендритный разветвление и нейрозащита после повреждения нейронов. Повышенные уровни IGF-I в сыворотке крови у детей были связаны с более высокими IQ.
IGF-1 формирует развитие улитка через контроль апоптоз. Его дефицит может вызвать слушание потеря. Уровень его в сыворотке также лежит в основе корреляции между короткими высота и снижение слуха, особенно в возрасте 3-5 лет и в возрасте 18 лет (позднее половое созревание).
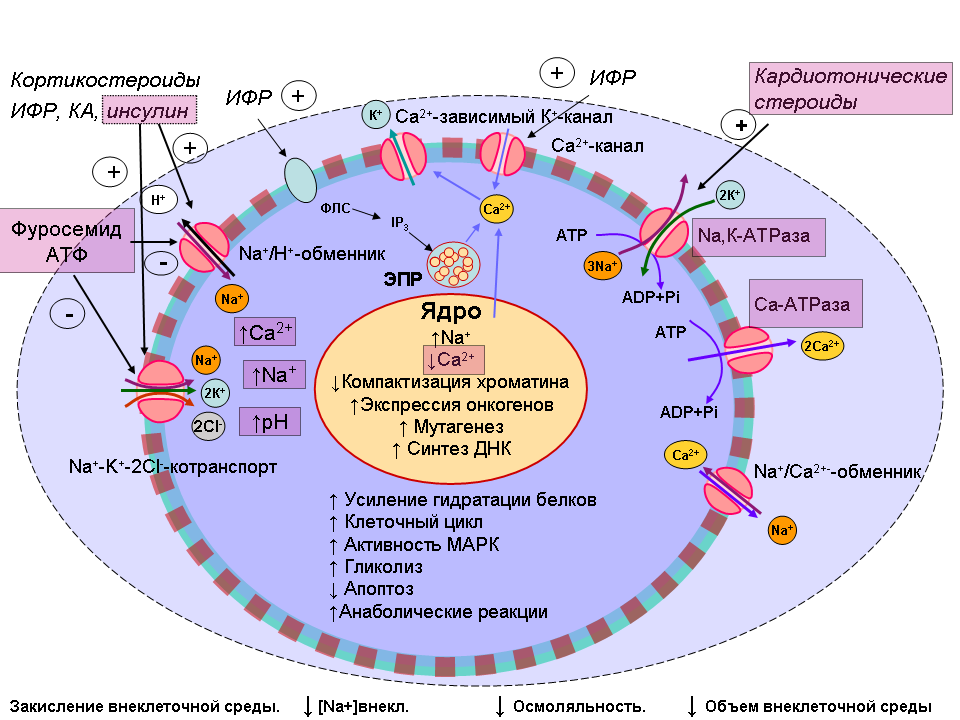
Инсулиноподобный фактор роста и инсулин
Жиросжигающие свойства ИФР-1 проистекают как раз из того, что он блокирует транспорт инсулином глюкозы через мембраны клеток, таким образом вынуждая организм переключиться на альтернативный источник энергии – жир. Впрочем, то же самое делают и кленбутерол (в несколько меньшей степени), и метформин (в большей степени – не только по отношению к кленбутеролу, но и к ИФР-1). По моему мнению, комбинация кленбутерола с метформином превосходит по силе (имеется в виду сжигание жира) инсулиноподобный фактор роста. В то же самое время гормон роста способен значительно усилить жиросжигающее действие ИФР-1 (скорее всего, за счет существенного продления периода полужизни ИФР-1).
Блокирование транспорта глюкозы сквозь мембраны мышечных волокон имеет и оборотную сторону – запасы гликогена в мышцах быстро иссякают и не пополняются, что, в конце концов, приводит к визуальному уменьшению размеров мышц и вполне конкретной потере выносливости. Для того, чтобы ликвидировать эти неприятные последствия, параллельно с инъекциями ИФР-1 делают инъекции инсулина. При схеме «через день» (инъекции инсулина делаются одновременно с инъекциями ИФР-1 каждый второй день) не происходит падения выносливости, а при ежедневных инъекциях выносливость даже повышается (что, впрочем, в значительной мере стоит «списать» на действие именно инсулина). Не происходит в этих случаях и визуального уменьшения размеров мышц (их массы), инъекции «через день» давали даже некоторый прирост мышечной массы, хотя и не такой значительной, как можно было бы ожидать.
Считается также, что инсулин несколько продлевает период полужизни ИФР-1, но не думаю, что настолько значительно, чтобы говорить об этом всерьез. Интересным мог бы стать эксперимент с ежедневными инъекциями инсулиноподобного фактора роста и инъекциями инсулина 1-2 раза в неделю. Можно было бы в эту схему включить также гормон роста (инъекции по схеме «через день» либо 3 раза в неделю). Мы такой эксперимент обязательно проведем.
Расстройства
Карликовость Ларона
Редкие заболевания, характеризующиеся неспособностью вырабатывать IGF-1 или реагировать на него, вызывают специфический тип нарушения роста. Одно из таких расстройств, называемое карликовостью Ларона, вообще не поддается лечению гормоном роста из-за отсутствия рецепторов GH. FDA сгруппировало эти заболевания в расстройство, называемое тяжелым первичным дефицитом IGF. Пациенты с тяжелым первичным IGFD обычно имеют нормальный или высокий уровень GH, рост ниже 3 стандартных отклонений (SD) и уровни IGF-1 ниже 3 SD. Тяжелый первичный IGFD включает пациентов с мутациями рецептора GH, пострецепторными мутациями или мутациями IGF, как описано ранее. В результате нельзя ожидать, что эти пациенты ответят на лечение GH.
Люди с синдромом Ларона очень редко заболевают раком и диабетом . Примечательно, что у людей с нелеченным синдромом Ларона также никогда не появляются прыщи.
Акромегалия
Акромегалия – это синдром, который возникает, когда передняя доля гипофиза вырабатывает избыток гормона роста (GH). Ряд заболеваний может увеличить выработку гормона роста гипофиза, хотя чаще всего это связано с опухолью, называемой аденомой гипофиза , происходящей из определенного типа клеток ( соматотрофов ). Это приводит к анатомическим изменениям и метаболической дисфункции, вызванным как повышенным уровнем GH, так и повышенным уровнем IGF-1. Высокий уровень IGF-1 при акромегалии связан с повышенным риском некоторых видов рака, особенно рака толстой кишки и рака щитовидной железы.
Рак
Мутация сигнального пути PI3K-AKT-mTOR является фактором образования опухолей, обнаруживаемых преимущественно на коже, внутренних органах и вторичных лимфатических узлах (саркома Капоши).
IGF-1R позволяет активировать эти сигнальные пути и впоследствии регулирует клеточное долголетие и метаболический повторный захват биогенных веществ. Терапевтический подход, направленный на уменьшение таких скоплений опухолей, может быть вызван ганитумабом . Ганитумаб представляет собой моноклональное антитело (mAb), антагонистически направленное против IGF-1R. Ганитумаб связывается с IGF-1R, предотвращая связывание IGF-1 и последующий запуск сигнального пути PI3K-mTOR; ингибирование этого пути выживания может привести к подавлению роста опухолевых клеток и индукции апоптоза опухолевых клеток.
Еще интересное о гормоне роста
У некоторых людей гормон роста способен повышать уровень пролактина. Учитывая тот факт, что из этих «некоторых» чувствительных к пролактину меньше трети, всерьез опасаться такого побочного эффекта вряд ли стоит. Но если он возникнет, его легко преодолеть с помощью бромокриптина («Парлодела»).
О наилучшем времени для инъекций. Период полужизни экзогенного гормона роста составляет от двух до четырех часов. Правда, о периоде полужизни в данном случае говорить не совсем корректно – это не совсем период полужизни в классическом понимании этого термина. Но что можно утверждать наверняка, так это то, что вводимый извне гормон роста подавляет секрецию организмом собственного на протяжении 4 часов (интересно, что уровень ИФР-1 после инъекции остается повышенным на протяжении 12-16 часов). Все сказанное делает нежелательным инъекции гормона роста перед сном – известно, что наибольший выброс собственного гормона роста происходит как раз через час-полтора после засыпания. Инъекция перед сном с успехом этот выброс подавит.
Может показаться – ничего страшного, выброса естественного ГР не будет, зато общий его уровень за счет введения извне останется высоким. Но подавление секреции организмом гормона роста, во-первых, крайне нежелательно (именно для того, чтобы избежать этого подавления, и прибегают к способу инъекций гормона роста через день, и практика подтверждает правоту такого подхода). А во-вторых, экзогенный ГР заменить эндогенный зачастую неспособен. Так что лучше прибегать к двум инъекциям гормона роста на протяжении дня: одну делать утром, вторую – после тренировки или в послеобеденное время.
Однако в условиях избыточной калорийности рациона, характерной для периода набора массы, гормон роста может одновременно провоцировать больший выброс инсулина. В этот же период существенно повышается и секреция ИФР-1 под влиянием гормона роста. В условиях пониженной калорийности рациона все происходит с точностью до наоборот.
Заболевания, вызванные IGF
Недавние исследования показывают, что ось инсулин / IGF играет важную роль в старение.Нематоды, плодовые мошки, и другие организмы имеют увеличенную продолжительность жизни, когда ген, эквивалентный инсулину млекопитающих, выбит. Однако связать это открытие с млекопитающими довольно сложно, потому что в меньшем организме есть много генов (по крайней мере 37 у нематод Caenorhabditis elegans), которые являются «инсулиноподобными» или «IGF-1-подобными», тогда как у млекопитающих инсулиноподобные белки состоят только из семи членов (инсулин, IGFs, релаксины, EPIL, и релаксиноподобный фактор)[нужна цитата]. Человеческие инсулиноподобные гены, по-видимому, играют разные роли с некоторыми, но меньшими перекрестными помехами, по-видимому, потому, что у людей есть несколько белков, подобных рецепторам инсулина. У более простых организмов обычно меньше рецепторов; например, у нематоды существует только один инсулиноподобный рецептор. C. elegans. Кроме того, C. elegans не имеют специализированных органов, таких как (Островки Лангерганса), которые воспринимают инсулин в ответ на гомеостаз глюкозы. Более того, IGF1 влияет на продолжительность жизни нематод, вызывая образование дауэра, стадии развития личинки C. elegans. Коррелятов у млекопитающих нет. Таким образом, вопрос о том, может ли IGF-1 или инсулин у млекопитающего нарушать старение, является открытым, хотя есть предположение, что это может быть связано с явлением ограничения питания.
Другие исследования начинают раскрывать важную роль IGFs в таких заболеваниях, как рак и сахарный диабет, показывая, например, что IGF-1 стимулирует рост как клеток рака простаты, так и рака груди. Исследователи не полностью согласны со степенью риска рака, которую представляет IGF-1.
Разница между гормоном роста и ИФР-1
Гормон роста влияет на синтез белка и рост мышечных волокон (а также связок, хрящей, костной ткани, внутренних органов) опосредствованно. Но – все через тот же инсулиноподобный фактор роста, синтезируемый под влиянием ГР в печени. Является ли он идентичным по действию тому рекомбинантному ИФР-1, который мы вводим в организм извне – большой вопрос. Скорее всего, нет. Является ли синтезируемый печенью IGF-1 идентичным по действию тому фактору роста, который образуется в клетках мышц, тоже вопрос. И ответ на него тоже, скорее всего, будет отрицательным. Гормон роста способен продлить период полужизни ИФР-1, но так ли это необходимо в случае и так достаточно «долгоживущего» Long R3 IGF-1, по крайней мере, если речь идет о наборе мышечной массы (о сжигании жира мы уже говорили несколько выше)? Возможно, продление периода полужизни инсулиноподобного фактора роста сверх необходимой меры сулит в этом плане больше отрицательных перспектив, нежели положительных, что пока что, кстати, подтверждается практикой.
Инсулиноподобный фактор роста может применяться и сам по себе (хотя показатели роста мышечной массы под влиянием ИФР-1 лежат в очень широких пределах – от совершенно ничтожных до выдающихся; при этом речь идет именно о «сухой» мышечной массе), а гормон роста требует для эффективной работы применения андрогенов. С другой стороны, показатели роста мышечной массы под влиянием комбинации андрогенов и гормона роста куда более стабильны. Кстати, недавний эксперимент, результаты которого изложены в статье «Geriatric Growth Hormone Interventions Not Ready For Clinical Use» (Journal Of the American Medical Association, 2002), показал, что пожилые люди могут добиваться прироста мышечной массы (существенного – до 3 кг за 26 недель) и при применении гормона роста «соло». Но возраст участников эксперимента составлял 65-88 лет, то есть, секреция собственного ГР у каждого из них была куда ниже нормы.